
据新华社北京4月14日消息(记者魏梦佳),北京大学邓宏魁团队经多年努力,成功开发化学小分子诱导技术使人成体细胞逆转为多潜能干细胞。

此为首次在国际上报道的、由我国自主研发的人多潜能干细胞(人CiPS细胞)制备技术,突破了以往干细胞制备技术的局限性,为我国干细胞和再生医学的发展解决了底层技术上的瓶颈问题,未来有望用于治疗糖尿病、重症肝病、恶性肿瘤等重大疾病。这一重要成果于4月13日在线发表于国际学术期刊《自然》。

CiPS细胞诱导技术
打开人类再生医学的大门
近年来,诱导多能干细胞技术的建立,在细胞治疗、药物筛选和疾病模型等领域产生了广泛的应用价值,尤其是为患者构建自体特异性干细胞系,大大加速了干细胞临床应用的进程。
多潜能干细胞在细胞治疗、药物筛选和疾病模型等领域具广泛应用价值,是再生医学领域最为关键的“种子细胞”。在哺乳动物发育过程中,其只短暂存在于胚胎发育的早期阶段,随后便会分化为构成生物体的各种类型的成体细胞,丧失其“种子细胞”特性。如何逆转这一自然发育过程,使高度分化的成体细胞重获早期多潜能状态,一直是干细胞与再生医学领域最重要的科学问题之一。
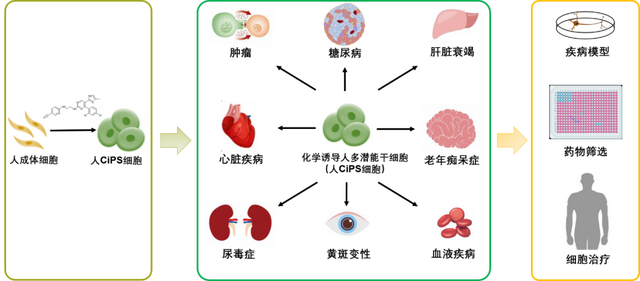
邓宏魁团队一直致力于开发调控细胞命运的新方法和建立制备干细胞的底层技术。受低等动物再生过程启发,团队发现高度分化的人成体细胞在特定化学小分子组合的诱导下,可以发生类似低等动物细胞可塑性变化。基于此发现,团队对化学小分子进行大量筛选和组合,最终成功诱导人CiPS细胞,实现人成体细胞发育过程的“逆转”。
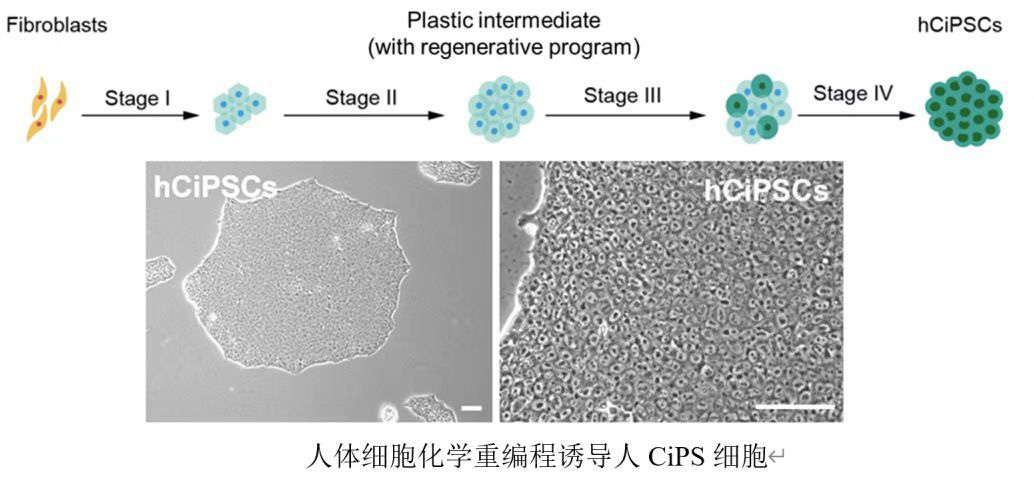
图片来自新华社微博
邓宏魁教授介绍,“这项全新技术,突破了以往干细胞制备技术的局限性,使干细胞制备更加简单安全、更易于标准化、更便于临床应用,为我国在再生医学和干细胞领域突破了一个瓶颈,为治疗重大疾病带来新的可能。”
实际上邓宏魁团队早在2013年,在小鼠的成体细胞上就建立了这样一个技术方法。
2013年,央视CCTV报道了邓宏魁教授及其团队带来的干细胞技术最新研究:采用化合物小分子的新方法,实现体细胞直接变成胚胎干细胞,途径更简捷,也更加安全。
邓宏魁教授团队的这项研究成果还被刊登在美国《Science》、《Cell》期刊上——《用小分子化合物诱导体细胞重编程为多潜能干细胞》。
研究团队认为生命现象的本质其实是化学,最有效改变的还是化学小分子。化学小分子重编程途径的优点是:时间缩短、效率提高、操作简单、性价比高、更为安全、可以精密调控。
这项诱导体细胞重编程获得多潜能干细胞的全新方法,是研究人员利用以四个小分子为主的小分子化合物组合对体细胞进行处理,成功逆转体细胞“发育时钟”,实现了体细胞的重编程,将已经特化的小鼠体细胞诱导成为可以重新分化发育为各种组织器官类型的多潜能性细胞,并将其命名为CiPS细胞。
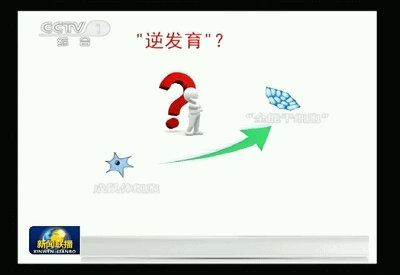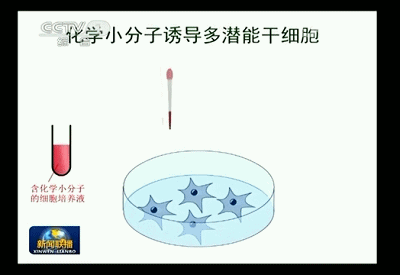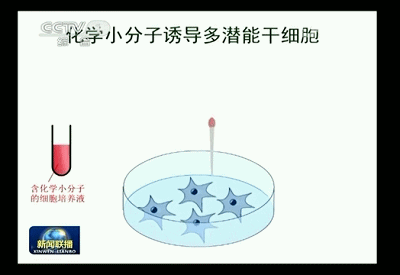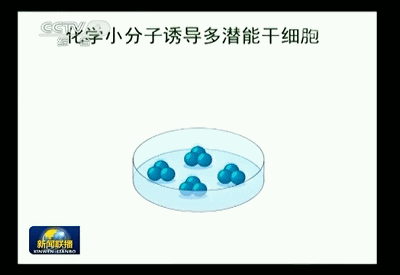
利用小分子化合物成功构建小鼠iPS细胞
利用这个方法,可以把小鼠的皮肤细胞重编程为多潜能干细胞,再将这个细胞打到小鼠的早期胚胎里,培养出活的小鼠。

研究团队使用4种小分子化学物质,将小鼠的皮肤细胞诱导成全能干细胞并克隆出后代,使用小分子化学物质替代病毒的新一代干细胞技术诞生
使用化学方法诱导体细胞重编程,摆脱了以往的重编程方法对遗传操纵的依赖,开启了对细胞新的认识。细胞发育过程具有可逆性,是可以受到转录因子和小分子调控的,改变细胞的状态,从而改变了细胞命运。现在理论上可以实现任何一种细胞在类型或功能上的功能转化。

这意味着细胞的生命时钟被成功地逆转了,让细胞恢复到了早期最原始、最强大的状态。这样的细胞可以继续分化为有具体功能的细胞或其他器官,从而可以为未来细胞治疗以及器官移植提供无限的可能。
人CiPS技术在生物医学领域
具备广阔的应用前景
现在,邓宏魁教授团队用这种化学小分子诱导成的新型种子干细胞,已进一步培养出了增强免疫力的人体血液T细胞和人体胰岛细胞,并且,人体胰岛细胞已经在大动物猴的身上取得实验成功,未来可用于治疗糖尿病。
对此,美国萨尔克研究所教授胡安·巴尔蒙蒂给予高度评价,“这将是再生医学领域的一项重大突破。因为没有用基因,他们用的是化学小分子重新编程。现在这就像吃一片阿司匹林一样,可控、高效地制备人体干细胞,用于重大疾病治疗,加快了进入临床应用的进程。”
——图文来自网络,如有侵权请联系删除